کاربرد نرم افزارهای آماری جهت صحه گذاری فرآیند برای برآوردهسازی اهداف سه گانه FDA
1- مقدمهای بر صحه گذاری فرآیند
اعتبارسنجی یا همان صحه گذاری فرایند برای موفقیت شرکتهایی که فرآوردهای دارویی، واکسنها، کیتهای آزمون و انواع دیگر محصولات بیولوژیک برای استفاده توسط انسان و یا حیوانات تولید میکند، حیاتی است. مطابق با دستورالعمل FDA، صحه گذاری فرایند به صورت زیر تعریف میشود:
“جمعآوری و ارزیابی دادهها، از چگونگی طراحی فرآیند برای تولید تجاری، که با شواهد علمی نشان میدهد که یک فرآیند قادر است به طور مداوم یک محصول با کیفیت ارائه نماید.”
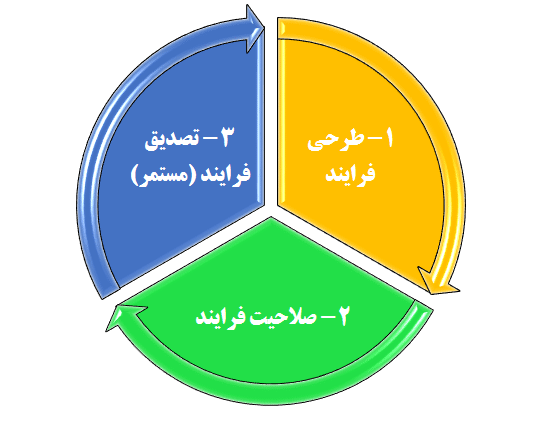
سازمان غذا و داروی آمریکا (FDA) سه مرحله نشان داده شده در نمودار زیر را برای اعتبارسنجی فرایند توصیه میکند. در ادامه این پست اهداف هر یک از مراحل و انواع فعالیتها و تکنیکهای آماری که معمولا برای هر یک از آنها استفاده میشود، تشریح خواهد شد. همچنین برای انجام تجزیه و تحلیلهای آماری میتوان از نرمافزارهای کنترل کیفیت آماری مانند minitab و یا Statgraphics استفاده نمود.
2- مرحله 1: طراحی فرایند
هدف: هدف این مرحله طراحی یک فرآیند مناسب برای ساخت تجاری روتین است که میتواند به طور مداوم محصولی را که با ویژگیهای کیفی آن مطابقت دارد، ارائه دهد. نشان دادن این که درک فرآیند درک شده است و مشخص کردن چگونگی پاسخ به ورودیهای مختلف در طراحی فرایند، مهم است.
مثال: شناسایی پارامترهای فرایندی مهم با طراحی آزمایشها (DOE)
فرض کنید شما نیاز به شناسایی پارامترهای فرآیندی مهم برای تولید یک قرص دارید. سه متغیر ورودی فرایند وجود دارد که میخواهید آنها را بررسی کنید:
1- اندازه ذرات (Particle size)؛
2- درصد تخریب کننده (dissolution %)؛
3- درصد پرکننده (filler %)؛
شما میخواهید تعیین کنید که هر یک از سه متغیر ورودی ذکر شده چه مقداری داشته باشند که بتوانید درصد انحلال قرص را در 30 دقیقه به حداکثر برسانید. طراحی آزمایشها (DOE) یک استراتژی جمعآوری دادهها را فراهم میکند. متغیرهای ورودیها به طور همزمان برای شناسایی روابط بین آنها و متغیر پاسخ مورد انتظار تنظیم میشوند. (برای کسب اطلاعات بیشتر در مورد طراحی آزمایش ها و انتخاب طرح آزمایش به پست مربوط به “چگونه طرح آزمایش مناسب را انتخاب نماییم؟” مراجعه نماید.)
انجام آزمایشها: اولین گام در طراحی آزمایشها DOE شناسایی متغیرهای ورودی و محدوده مربوطه به آنها است که میخواهید با استفاده از آنها پاسخ بهینه را بیابید. سپس بایستی یک طرح آزمایش ایجاد کرد که به عنوان طرح جمع آوری داده های برای شما عمل میکند.
برای مثال مطابق با طرح آزمایش نشان داده شده در جدول زیر، در اولین آزمایش
1- اندازه ذرات برابر با 10؛
2- درصد تخریب کننده برابر با 1؛ و
3- درصد MCC برابر با 33.3 در نظر گرفته میشود.
آزمایش اول با توجه به شرایط مشخص شده انجام میشود و نتایج بدست آمده از آن در جدول زیر ثبت میشود.
آزمایشات دیگر نیز مطابق با جدول فوق انجام میشود و نتایج آنها ثبت میشود و بر اساس نتایج بدست آماده نمودار پارتو زیر را رسم میکنیم
تجزیه و تحلیل دادهها: با استفاده از تجزیه و تحلیل آزمایشها DOE و مقادیر p-values، میتوانیم متغیرهای ورودی مهم فرایند را شناسایی نمود. برای مثال ارائه شده متغیرهای ورودی که در نمودار پارتو مشخص شدهاند (متغیرهای مهم، متغیرهای هستند که مقدار آنها از حد بحرانی (خط چین قرمز) بیشتر است). بر این اساس میوان نتیجه گرفت که اندازه ذارت و درصد تخریب کننده و همچنین اثر متقابل بین دو متغیر اندازه ذرات و درصد تخریب کننده به طور معناداری درصد انحلال قرص را تحت تاثیر قرار میدهند ولی متغیر درصد پرکننده تاثیر معناداری بر روی درصد انحلال قرص ندارد.
بهینه سازی کیفیت محصول: پس از تعیین میزان تاثیر متغیرهای ورودی، میتوان با بهینه سازی مقادیر بهینه برای هر یک از متغیرهای ورودی را تعیین کنیم با رسم یک نمودار سطح (contour plot) برای دو متغیر تاثیرگذار اندازه ذارت و درصد تخریب کننده میتوان به راحتی مقادیر بهینه برای متغیرهای ورودی به رسیدن به پاسخ بهینه (درصد انحلال 80% یا بیشتر) را تعیین نمود.
3- مرحله 2: صلاحیت فرآیند
اهداف: هدف از این مرحله ارزیابی آن است که فرایند طراحی شده قابلیت تولید تجاری تجدیدپذیر را دارد یا خیر. انجام این ارزیابی پیش از شروع به تولید در سطح تجاری ضروری است.
مثال 1: ارزیابی معیارهای پذیرش را با تحلیل قابلیت یا توانایی فرایند
فرض کنید مقدار ماده موثر در یک آرام بخش باید بین 360 تا 370 میلیگرم بر میلیلیتر باشد و شما باید سطح کیفیت را ارزیابی کنید، در جایی که مقدار Cpk بزرگتر از 1.33 به عنوان معیار پذیرش تعریف شده است. برای ارزیابی عملکرد فرایند و تعیین اینکه آیا نمونههای مورد اندازه گیری در درون حدود مشخصات هستند، از تجزیه و تحلیل قابلیت فرایند استفاده شده است. پنج نمونه به صورت تصادفی از 50 بچ انتخاب شده و مقدار ماده موثر آنها اندازهگیری میشود. سپس داده ها با توجه به حدود مشخصات (حداقل 360mg/mL و حداکثر 370mg/mL) تجزیه و تحلیل میشود.
پس از انجام تجزیه و تحلیل قابلیت فرایند Cpk= 0.53 بدست آمده است که با مقدار قابل قبول آن یعنی 1.33 فاصله زیادی دارد. بر این اساس میتوان نتیجه گرفت که مقادر ماده موثره موجود در آرامبخش قابل قبول نمیباشد. سئوالی که اینک مطرح میشود آن است که چگونه میتوان آن را بهبود داد؟
همانطور که در نمودار رسم شده مشاهد میشود مقدار Cp = 1.41 است. این امر نشان دهنده آن است که تغییرپذیری فرایند (پراکندگی میان محصولات) قابل قبول میباشد ولی میانگین فرایند مناسب نیست. به منظور دستیابی به Cpk قابل قبول، میانگین فرایند باید افزایش یاد.
مثال 2: تحليل تغييرات در بین بچها با نمودار جعبهای (boxplots) زیر نشان داده شده است.
فرض کنید میخواهیم یکنواختی بچها را به عنوان یک مشخصه کیفیت بحرانی در سه بچ در 10 مکان مختلف بررسی کنیم. برای تجسم تغییرپذیری درون یک بچ و تغییرپذیری بین بچها و شناسایی مشاهدات پرت، ما میتوانیم نمودار جعبهای (boxplots) را برای هر بچ رسم کنیم. برای مثال ارائه شده نمودار رسم شده نشان میدهد که پراکندی نتایج بدست آمده در درون بچها و همچنین بین بچها تقریباً یکسان (هموژن) است و هیچ گونه داده پرتی وجود ندارد. (در نرم افزار minitab بر روی نمودار جعبهای اگر داده پرتی وجود داشده باشد، با علامت (*) نشان داده میشود.
اگر چه نمودار جعبهای boxplots ابزار مفید برای انجام یک ارزیابی بصری است، ولی یک تحلیل آماری جهت بررسی فرضیه یکسان بودن پراکندگی بین بچها را به ارائه نمیدهد. برای انجام این کار میتوانیم از آزمون آماری بررسی برابری واریانسهای استفاده نمود. این آزمون به ما خواهد گفت که آیا اختلاف قابل توجهی در بین تغییرپذیری (پراکندگی مشاهدات) بین بچها وجود دارد یا خیر. آزمون بررسی یکسان بودن پراکندگی نتایج نشان میدهد در سطح اطیمنان مشخص (معمولاً 95%) آیا پراکندگی مشاهدات در میان بچها اختلاف معناداری با یکدیگر دارند یک خیر. (اگر p-value بزرگتر از مقدار آلفا 0.05 باشد، اختلاف معناداری وجود ندارد.)
مثال 3: کاربردهای مختلف برای حدود رواداری
یکی دیگر از ابزارهای مفید برای بررسی صلاحیت فرایند، تعیین فاصله رواداری است. این ابزار دارای کاربردهای متعدد است. به عنوان مثال، فواصل رواداری میتواند برای مقایسه فرآیند شما با مشخصات، نمایش نتیجه یک فرآیند یا ایجاد معیارهای پذیرش استفاده شود.
برای یک مشخصه محصول داده شده، یک فاصله رواداری محدوده ای از مقادیر را فراهم میکند که احتمالاً نسبت مشخصی از جمعیت (به عنوان مثال 95٪) برای سطح اطمینان مشخص شده (مانند 99٪) را پوشش میدهد.
به عنوان مثال، فرض کنید ما میخواهیم بدانیم که چقدر مقدار از مواد موثر مورد استفاده برای تولید یک آرامبخش، در فرآیند تولید در محدود مشخصات معینی است. حدود مشخصات در این مثال بین 360 تا 370 میلیگرم بر میلیلیتر است.
برای این مجموعه اطلاعات خاص، Minitab نشان میدهد که میتوانیم با اطمینان 99٪ گفت که 95٪ از اقلام بین 362.272 و 367.468 میلیگرم در میلیلیتر میباشند. مرزهای فرایند نشان میدهد که ما میتوانیم الزامات 360 تا 370 را برآورده کنیم و ما میتوانیم با اطمینان بالا نتیجهگیری کنیم که تغییرپذیری فرایند کمتر از تغییرپذیری مجاز تعریف شده است.
4- مرحله 3: تصدیق فرآیند به صورت مستمر
اهداف: این مرحله از کار به صورت مدوام این اطمینان را ایجاد میکند که فرایند در حین تولید تجاری در حالت تحت کنترل (وضعیت صحهگذاری شده) باقی میماند.
مثال: پایش یک فرآیند با نمودارهای کنترل
فرض کنید شما مسئول پایش یک فرایند تولید قرص خوراکی هستید. شما باید نشان دهید که سختی محصولات در طول زمان پایدار است و تشخیص دهید که آیا تغییرپذیری فرایند تغییر کرده است یا خیر. شما همچنین میخواهید اطمینان حاصل کنید که اپراتورهای خط تولید به تغییرات جزئی در داده ها (که در تغییرات ذاتی فرایند هستند) پاسخ بیش از حد نمیدهند. اجتناب از پاسخ بیش از حد مانع از تنظیمات غیر ضروری فرایند میشود که ممکن است در واقع باعث افزایش غیرمتمرکز تغییرپذیری شود.
شما پنج قرص را در ساعت بر میدارید، سختی آنها را اندازهگیری میکنید و سپس یک نمودار کنترل Xbar-R رسم میکنید.
در این نمودار Xbar-R هیچ نقطهای را با رنگ قرمز نشان داده نشده است و بنابراین نشان میدهد که این فرایند تحت کنترل آماری است. شما میتوانید نتیجه بگیرید که عملکرد فرایند همچنان مناسب است و تغییرات ناخواسته و غیر معمول در میانگین فرآیند (نمودار Xbar ) و یا تغییرات پرداکندگی مشاهدات (نمودار R) وجود ندارد .
اگر نمودار کنترلی حالت خارج از کنترلي را نشان دهد، میتوان نتیجه گرفت که فرآيند در معرض منابع تغییرپذیری غير منتظره (عوامل اکتسابی) قرار دارد، مراحل بعدی شامل مشخص کردن علت ایجاد مشکل و انجام اقدامات اصلاحی است. بدین منظور باید بررسی شود که:
- آیا مشکل ناشی از تغییر در مواد است؟
- آیا مشکل ناشی نگهداری یا کالیبراسیون تجهیزات است؟
- یا آیا منبع دیگری از تغییرپذیری وجود دارد، که موجب تغییر فرایند شده است؟
تشخیص تغییرات نامطلوب در فرایند میتواند با پایش و کنترلهای معمول انجام شود.
علاوه بر نمودارهای کنترل که معمولاً برای پایش فرایند استفاده میشوند ابزارهای آماری مفید دیگری نیز وجود دارند که برای تصدیق فرایند به شما کمک میکند. به عنوان مثال نمونه برداری پذیرشی یکی از ابزارهای مناسب است که با استفاده از آن میتوانید تعداد نمونه مورد نیاز برای تایید یا رد یک انباشه (بچ یا بهر) را تعیین کنید. در پایان یادآوری میشود که استفاده از نرم افزارهای کنترل کیفیت آماری مانند minitab و یا Statgraphics برای بررسی و صحهگذاری فرایند در مراحل مختلف به شما میتواند کمک قابل توجهای نماید.
5- برگزاری دوره آموزشی کنترل فرایند آماری با نرم افزار:
جهت هماهنگی برای برگزاری “دوره آموزش کنترل فرایند آماری (SPC)” و “دوره آموزش طراحی و تحلیل آزمایشها” میتوانید با ما تماس بگیرید.









دیدگاهتان را بنویسید